Índice
- 1. Introdução: A Ciência por Trás do Ato Cotidiano de Limpar
- 2. Fundamentos Químicos Essenciais: O Princípio “Semelhante Dissolve Semelhante”
- 2.1. A Força da Polaridade Molecular
- 2.2. Interações Moleculares e Solubilidade: A Regra de Ouro da Química da Limpeza
- 3. Os Veículos de Limpeza: Uma Classificação Essencial
- 3.1. Água: O Solvente Universal e suas Limitações Intrínsecas
- 3.2. O Papel dos Agentes Tensoativos (Sabões e Detergentes)
- 4. Solventes Polares e Apolares em Ação: Casos de Uso Práticos
- 4.1. Solventes Polares Comuns: O Álcool, a Acetona e a Dupla Mágica do Bicarbonato
- 4.2. O Poder dos Solventes Apolares: Aplicações Industriais e Domésticas Específicas
- 4.3. Tabela Comparativa de Propriedades Físico-Químicas
- 5. Segurança, Toxicidade e Boas Práticas no Manuseio de Solventes
- 5.1. Riscos para a Saúde Humana e o Meio Ambiente
- 5.2. O Papel Essencial da Ficha de Informações de Segurança de Produto Químico (FISPQ)
- 5.3. Diretrizes para um Manuseio Seguro
- 6. Sustentabilidade e o Ciclo de Vida dos Solventes
- 6.1. O Impacto Ambiental do Descarte Incorreto
- 6.2. A Economia Circular dos Solventes
- 6.3. Alternativas Ecológicas e Biodegradáveis
- 📌 7. Conclusão e Recomendações: A Escolha do Veículo Perfeito
- 📚 Bibliografia
- Glossário:
A limpeza é um processo diário, mas a sua eficácia depende de princípios químicos complexos que regem a interação entre substâncias.
A escolha do veículo de limpeza adequado – seja ele a água, um detergente ou um solvente especializado – é uma decisão multifatorial, baseada não apenas na eficácia, mas também na segurança, na toxicidade e no impacto ambiental.
Este relatório tem como objetivo desvendar os fundamentos da polaridade molecular e da solubilidade, traduzindo-os em um guia prático para a seleção criteriosa de agentes de limpeza.
Aborda a química por trás da ação de sabões e detergentes, a aplicação de solventes polares e apolares em contextos domésticos e industriais, e discute as implicações críticas de segurança e as melhores práticas de sustentabilidade, incluindo a reciclagem de solventes e o uso de alternativas ecológicas.
A análise conclui que a tomada de decisão informada requer a compreensão dos fundamentos químicos e a consulta a fontes de informação técnica, como a Ficha de Informações de Segurança de Produto Químico (FISPQ), para garantir a segurança e a responsabilidade.
1. Introdução: A Ciência por Trás do Ato Cotidiano de Limpar
O ato de limpar, seja uma panela engordurada, uma peça mecânica ou uma superfície manchada de tinta, é percebido no cotidiano como uma tarefa simples.
No entanto, por trás dessa simplicidade aparente, opera uma série de princípios da química que definem a eficácia de cada método.
A capacidade de uma substância se dissolver em outra, um conceito conhecido como solubilidade, é o alicerce de todo processo de limpeza química.
A compreensão de por que certas substâncias se misturam e outras se repelem não é apenas uma curiosidade acadêmica; é o conhecimento fundamental que permite a otimização de processos, a garantia de segurança e a minimização de danos ambientais.
Este relatório busca preencher a lacuna entre o conhecimento intuitivo e a base científica, fornecendo uma análise técnica e didática que capacita o leitor a fazer escolhas informadas, guiadas pela ciência.
2. Fundamentos Químicos Essenciais: O Princípio “Semelhante Dissolve Semelhante”
2.1. A Força da Polaridade Molecular
A pedra angular da solubilidade reside na propriedade das moléculas conhecida como polaridade.1 Uma molécula é considerada polar quando apresenta uma distribuição interna de cargas assimétrica, resultando em regiões parcialmente positivas e negativas.2
Este desequilíbrio de carga é frequentemente causado pela diferença de eletronegatividade entre os átomos que compõem a molécula. A água (H2O) é o exemplo mais clássico de uma molécula polar.2
A sua geometria molecular em “V” e a forte eletronegatividade do átomo de oxigênio em relação aos átomos de hidrogênio geram um dipolo elétrico permanente, com o oxigênio possuindo uma carga parcial negativa e os hidrogênios cargas parciais positivas.5
Em contraste, as moléculas apolares, como os óleos e a gasolina, são formadas por ligações cujas cargas são distribuídas de maneira uniforme.1
A atração entre as moléculas de óleo é fraca, mas a ausência de polos de carga impede que elas interajam favoravelmente com moléculas polares, resultando na sua repulsão mútua.6
2.2. Interações Moleculares e Solubilidade: A Regra de Ouro da Química da Limpeza
O princípio fundamental que governa a solubilidade é a regra “semelhante dissolve semelhante”.7 Isso significa que compostos polares são mais facilmente dissolvidos em solventes polares, e compostos apolares em solventes apolares.7
A explicação para este princípio não se limita a uma simples atração. A realidade molecular envolve uma competição entre as forças de atração intermoleculares. Moléculas polares, como a água, exercem fortes forças de coesão entre si, conhecidas como ligações de hidrogênio.6
Para que a água possa dissolver um soluto, essas interações fortes devem ser superadas por interações favoráveis entre as moléculas de água e as partículas do soluto.7 Quando um soluto polar (como o sal de cozinha, cloreto de sódio) é adicionado à água, as moléculas de água, que são dipolos, orientam suas extremidades de carga oposta em direção aos íons do sal, atraindo-os e quebrando a sua estrutura cristalina. Este processo de solvatação é energeticamente favorável.7
No entanto, quando se tenta misturar água com uma substância apolar, como o óleo, a dinâmica muda.6 As moléculas de água continuam a preferir interagir entre si através de suas fortes ligações de hidrogênio.
A atração que as moléculas de água poderiam ter com o óleo é insignificante em comparação com as interações H₂O-H₂O. Como resultado, as moléculas de água se aglomeram, empurrando as moléculas de óleo para fora da mistura e forçando-as a se agruparem em uma fase separada.
O que para o leigo é a “não mistura” de água e óleo, é na verdade a água preferindo interagir consigo mesma, uma demonstração da predominância das forças intermoleculares polares.3
3. Os Veículos de Limpeza: Uma Classificação Essencial
3.1. Água: O Solvente Universal e suas Limitações Intrínsecas
A água é frequentemente apelidada de “solvente universal” devido à sua notável capacidade de dissolver uma vasta gama de substâncias.8 Suas propriedades polares a tornam um excelente solvente para compostos polares e iônicos, como sais (cloreto de sódio) e açúcar.7 Experiências cotidianas, como a dissolução de sal em água, servem como uma demonstração direta e acessível do princípio “semelhante dissolve semelhante”.7
No entanto, o caráter polar da água também é a causa de sua maior limitação como agente de limpeza: a incapacidade de interagir com e dissolver sujidades apolares, como óleos, graxas e gorduras.5 Para superar essa barreira, a química moderna recorre a uma categoria de substâncias conhecidas como tensoativos.
3.2. O Papel dos Agentes Tensoativos (Sabões e Detergentes)
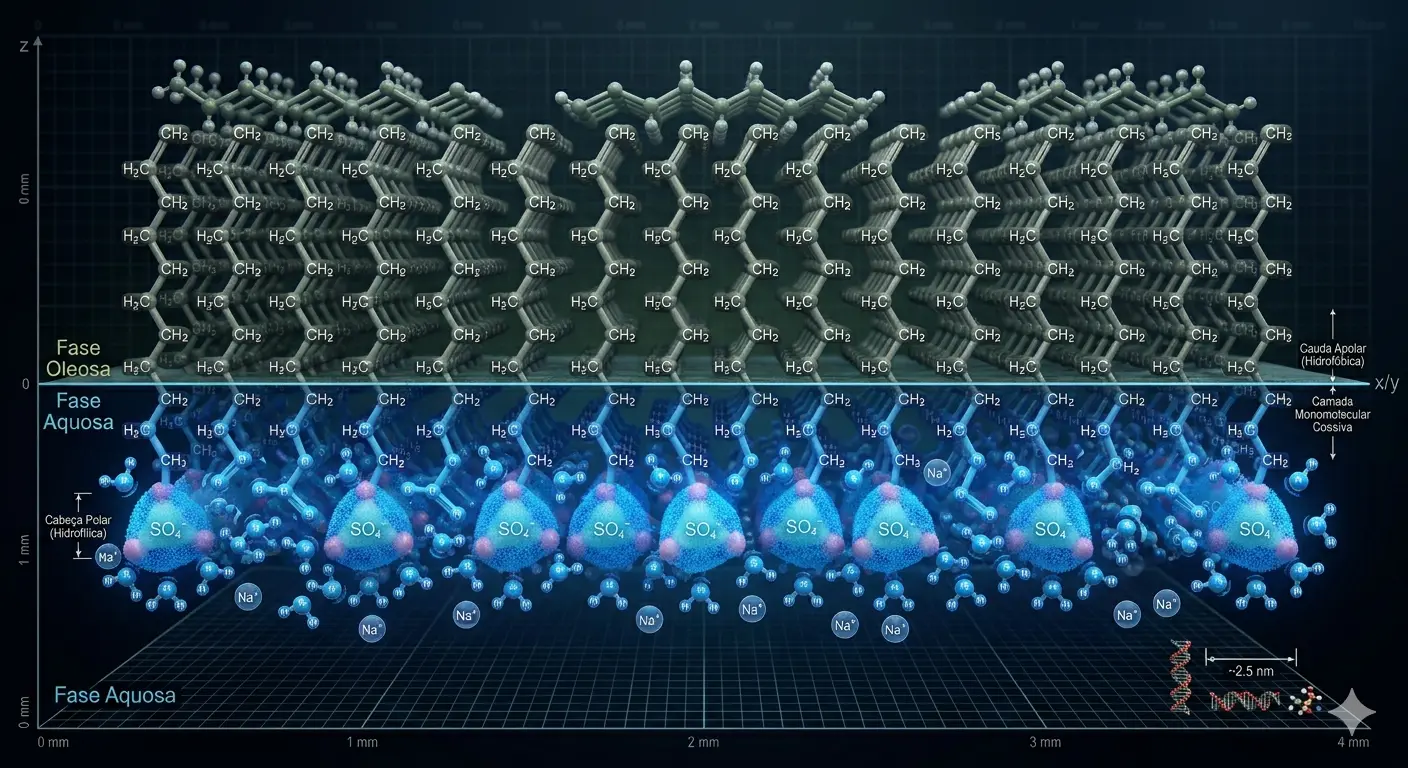
A ineficácia da água na remoção de gorduras é um desafio superado pelos agentes tensoativos, como sabões e detergentes.5 A grande descoberta por trás da sua eficácia reside na sua natureza anfifílica, o que significa que as moléculas desses compostos possuem uma dualidade: uma parte polar (hidrofílica, ou “amiga da água”) e uma parte apolar (hidrofóbica ou lipofílica, que interage com a gordura).5
O mecanismo de ação dos tensoativos é uma sinergia entre a redução da tensão superficial e a emulsificação da sujeira. A água possui uma alta tensão superficial, o que impede que ela penetre em pequenos poros e ranhuras, dificultando a limpeza.5
Quando o sabão ou o detergente é adicionado, a parte polar de suas moléculas se alinha na superfície da água, rompendo as ligações de hidrogênio e, assim, diminuindo a tensão superficial.5 Isso permite que a água “molhe” a superfície de forma mais eficaz e penetre em áreas de difícil acesso.
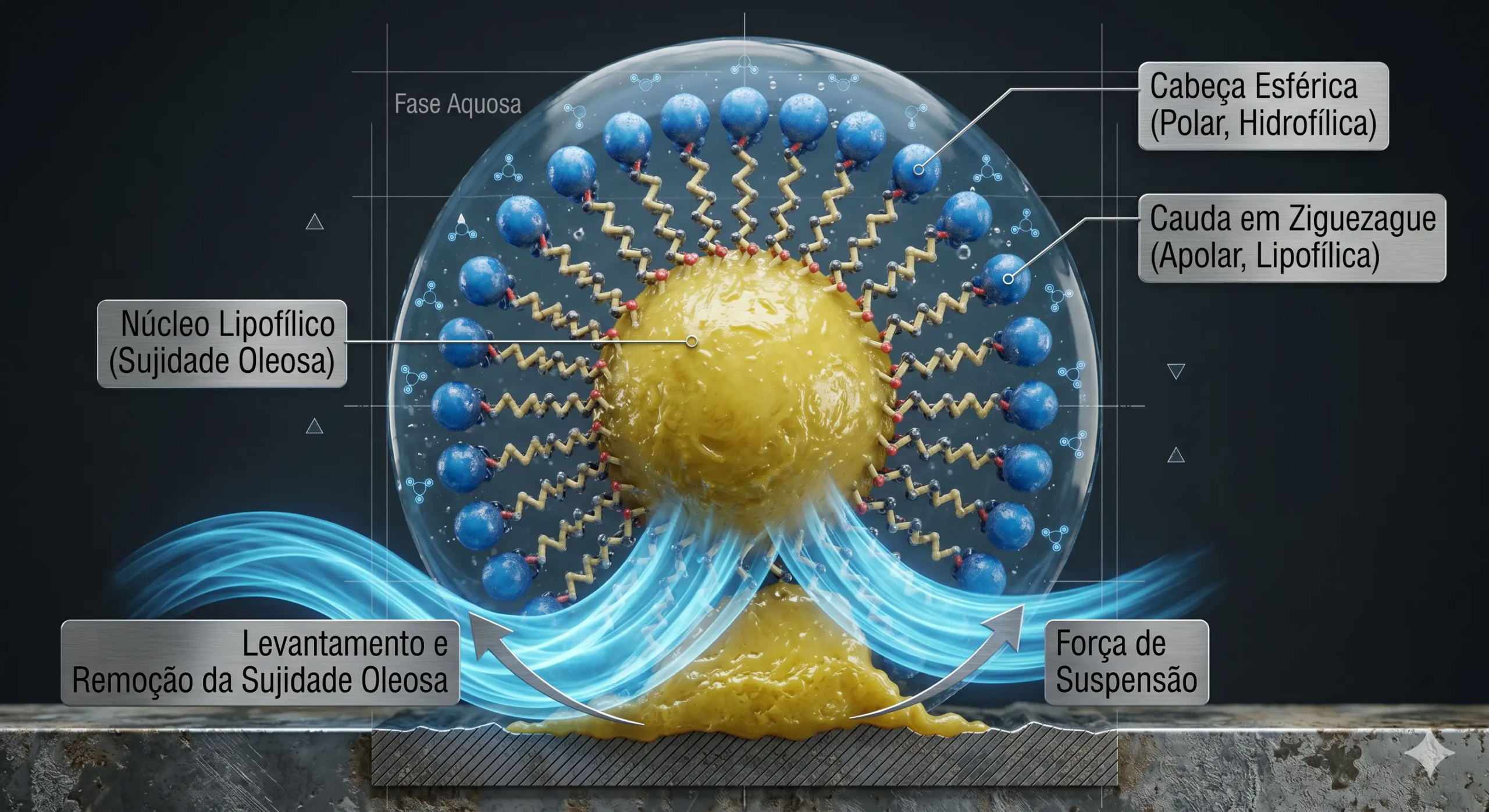
Simultaneamente, o tensoativo inicia o processo de emulsificação. A parte apolar da molécula se sente atraída e interage com as sujidades apolares, como óleos e gorduras. Em solução aquosa, as moléculas de sabão e detergente se agrupam em estruturas esféricas microscópicas chamadas micelas.5
Nessas micelas, as partes apolares das moléculas se voltam para o interior, encapsulando a sujeira gordurosa, enquanto as cabeças polares ficam voltadas para o exterior, em contato com as moléculas de água. Essa configuração permite que a gordura, agora aprisionada no centro da micela, seja suspensa e removida pela água, superando a incompatibilidade inicial.5
Este mesmo princípio é utilizado na indústria de alimentos e cosméticos, onde emulsificantes—moléculas anfifílicas—são usados para misturar líquidos imiscíveis, como água e óleo, na produção de maioneses e sorvetes.15 A onipresença desse mecanismo químico demonstra sua eficácia e versatilidade.
4. Solventes Polares e Apolares em Ação: Casos de Uso Práticos
4.1. Solventes Polares Comuns: O Álcool, a Acetona e a Dupla Mágica do Bicarbonato
Enquanto a água é o solvente polar mais onipresente, outros solventes com polaridades distintas são essenciais para a limpeza de sujidades específicas. A acetona (CH3COCH3) é um solvente orgânico polar que se destaca pela sua eficácia na remoção de substâncias como resinas, tintas e esmaltes.16 Sua alta polaridade permite que ela dissolva rapidamente os polímeros e aditivos presentes nos esmaltes de unha, facilitando a sua remoção com a aplicação de algodão e papel alumínio.16 A acetona também é eficaz em muitas outras gorduras e éteres.17
O álcool etílico (C2H5OH) é outro solvente polar amplamente utilizado na limpeza doméstica. Embora seja menos polar que a água, a sua cadeia de hidrocarboneto confere-lhe uma capacidade de interagir com certas gorduras, tornando-o um solvente versátil para superfícies, como vidros e bancadas.19 A sua volatilidade também contribui para uma secagem rápida, o que evita a formação de manchas.19
A mistura de bicarbonato de sódio e vinagre exemplifica uma combinação de agentes de limpeza de naturezas opostas que criam uma sinergia de ação. O vinagre (CH3COOH) é um ácido, enquanto o bicarbonato de sódio (NaHCO3) é uma base.21
Quando misturados, eles reagem de forma efervescente, produzindo acetato de sódio, água e dióxido de carbono.22 O bicarbonato atua como um abrasivo suave, auxiliando na remoção mecânica de resíduos, enquanto o vinagre age como um solvente polar para gorduras e manchas.21 A combinação é especialmente útil para desentupir ralos e limpar superfícies incrustadas.21
4.2. O Poder dos Solventes Apolares: Aplicações Industriais e Domésticas Específicas
Para sujeiras que desafiam a água e os sabões, como óleos pesados, vernizes e tintas à base de solvente, os solventes apolares são a única escolha viável.23 Compostos como o thinner de limpeza industrial, que é uma mistura de hidrocarbonetos apolares, são formulados especificamente para dissolver resíduos apolares de forma rápida e completa.23
A regra “semelhante dissolve semelhante” se aplica perfeitamente aqui: a natureza apolar do solvente é a chave para a remoção eficaz da sujeira apolar.9
A limpeza à base de solventes é um método versátil, conhecido como “limpeza a frio”, e é empregado em diversas aplicações industriais para otimizar processos de fabricação e aumentar a produtividade.23 É adequado para a limpeza de uma variedade de materiais, incluindo metal, plástico, vidro e cerâmica.23
Exemplos práticos incluem a limpeza química de tanques, o desengraxamento de peças de máquinas e a remoção de resíduos de vernizes e tintas.23 Métodos como a imersão total do objeto em um tanque de limpeza ou a pulverização de alta pressão são utilizados para garantir a completa remoção das impurezas.23
4.3. Tabela Comparativa de Propriedades Físico-Químicas
A análise das propriedades físico-químicas de solventes comuns é um passo crucial para a escolha informada de um veículo de limpeza. A tabela a seguir consolida dados essenciais que quantificam a polaridade, volatilidade e outras características de alguns dos solventes discutidos. Esses dados são fundamentais para avaliar não apenas a eficácia, mas também os riscos de segurança, como a inflamabilidade.
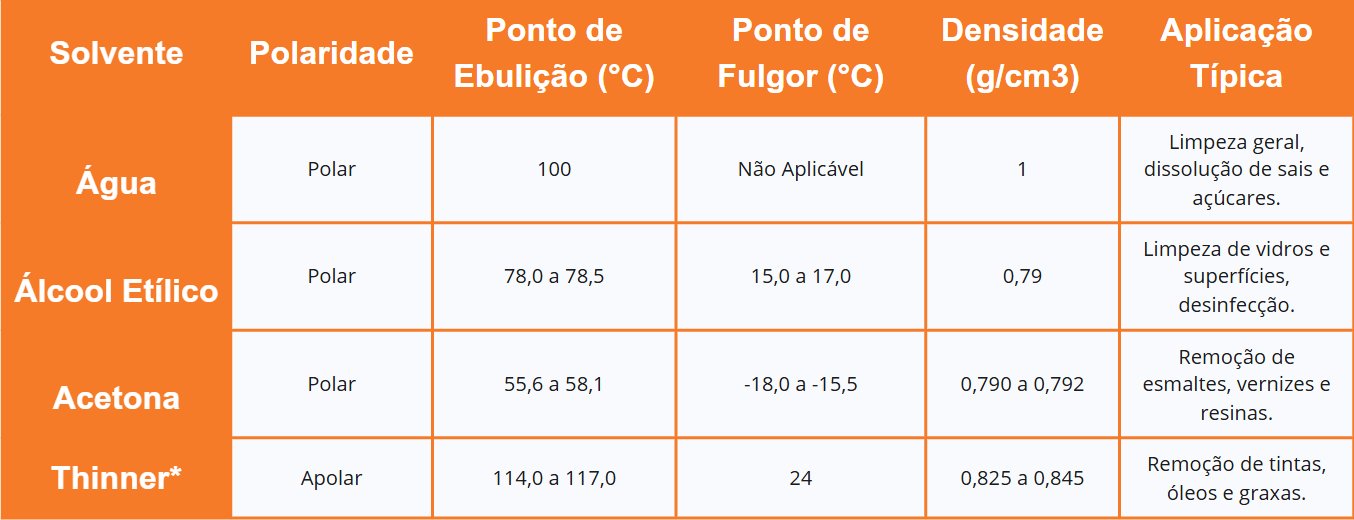
*O thinner de limpeza industrial é uma mistura de solventes apolares, e os dados variam. Os valores na tabela são exemplares e baseados em um tipo comum de thinner.
5. Segurança, Toxicidade e Boas Práticas no Manuseio de Solventes
5.1. Riscos para a Saúde Humana e o Meio Ambiente
O uso de solventes, apesar de sua eficácia, não é isento de riscos significativos para a saúde humana e o meio ambiente.
A volatilidade de muitos solventes permite que seus vapores se dispersem no ar, sendo inalados e absorvidos pelo corpo.26 Sua natureza lipossolúvel os torna capazes de se acumular em tecidos gordurosos do corpo, como o sistema nervoso, e de atravessar a barreira hematoencefálica.26
A exposição a solventes como a acetona pode levar à depressão do sistema nervoso central, causando letargia, tontura e, em casos graves, coma.28 Outros solventes, como o benzeno e o tricloroetileno, são classificados como carcinogênicos, aumentando o risco de doenças graves.27 A natureza tóxica e inflamável desses compostos exige o máximo de cautela em seu manuseio.26
5.2. O Papel Essencial da Ficha de Informações de Segurança de Produto Químico (FISPQ)
A eficácia de um solvente muitas vezes ofusca os perigos inerentes a seu uso. No contexto doméstico e até mesmo em pequenas operações industriais, os usuários são expostos a produtos perigosos sem o devido conhecimento ou acesso a informações cruciais para um manuseio seguro.
A Ficha de Informações de Segurança de Produto Químico (FISPQ), conhecida internacionalmente como Material Safety Data Sheet (MSDS) ou Safety Data Sheet (SDS), é o documento técnico e legal que mitiga esse risco.30
A FISPQ é uma fonte de dados indispensável que fornece procedimentos para a manipulação segura de substâncias, incluindo dados físicos e toxicológicos, instruções de primeiros socorros, procedimentos para combate a incêndio, manuseio, armazenamento e descarte, e a identificação de equipamentos de proteção individual (EPIs) necessários.30
A consulta a este documento deve preceder a escolha e a utilização de qualquer produto químico, pois ele é a única fonte de informações quantificáveis sobre os riscos e as medidas de controle necessárias, indo além de uma mera recomendação de segurança.30
5.3. Diretrizes para um Manuseio Seguro
O manuseio seguro de solventes requer a adesão rigorosa a diretrizes de segurança. É fundamental utilizar os Equipamentos de Proteção Individual (EPIs) adequados, como luvas, óculos de proteção e máscaras respiratórias, especialmente em ambientes com pouca ventilação.25
A ventilação do ambiente de trabalho, seja ela natural ou através de exaustores, é crucial para evitar a formação de misturas explosivas e a inalação de vapores tóxicos.25
O armazenamento correto, em embalagens originais, bem vedadas e longe de fontes de calor, faíscas ou luz solar direta, é essencial para manter as propriedades do produto e prevenir acidentes.25
Além disso, a mistura de solventes com outros produtos químicos deve ser evitada a todo custo, pois pode desencadear reações perigosas e comprometer a segurança do usuário.25
6. Sustentabilidade e o Ciclo de Vida dos Solventes
6.1. O Impacto Ambiental do Descarte Incorreto
O uso de solventes, tanto em nível industrial quanto doméstico, acarreta uma responsabilidade ambiental significativa. O descarte incorreto de resíduos contendo solventes, seja em pias, bueiros ou diretamente no lixo e no solo, é uma das principais causas de contaminação ambiental.27
A natureza tóxica e lipossolúvel desses compostos permite que eles se infiltrem e contaminem o solo e os lençóis freáticos, com consequências catastróficas para a biodiversidade e a saúde pública.27 Além disso, a volatilidade dos solventes resulta na emissão de Compostos Orgânicos Voláteis (VOCs), que são poluentes atmosféricos nocivos.37
6.2. A Economia Circular dos Solventes
A gestão responsável de solventes na indústria está diretamente ligada à promoção de uma economia circular. A reciclagem de solventes é uma prática sustentável que não apenas minimiza o impacto ambiental, mas também oferece benefícios econômicos tangíveis.37
A recuperação de solventes usados reduz a quantidade de resíduos perigosos que necessitam de descarte, o que, por sua vez, diminui os custos de eliminação para as empresas.37
O processo de reciclagem mais comum é a destilação.38 Este método envolve o aquecimento do solvente contaminado até seu ponto de ebulição, convertendo-o em vapor e separando-o das impurezas não voláteis, que permanecem no estado líquido.38 O vapor é então resfriado em um condensador, retornando ao estado líquido em uma forma purificada, pronta para ser reutilizada no mesmo ou em outro processo produtivo.41
A adoção da reciclagem de solventes por destilação representa um avanço em sustentabilidade que vai além da responsabilidade ambiental. A produção de solventes a partir de matérias-primas virgens é um processo de uso intensivo de energia, que consome recursos naturais e emite gases de efeito estufa.
Em contraste, a destilação de solventes usados requer significativamente menos energia, o que resulta em uma redução da pegada de carbono e promove a conservação de matérias-primas e recursos hídricos.37 Além disso, os sistemas de recuperação em circuito fechado capturam e controlam os VOCs, impedindo sua liberação na atmosfera.37
6.3. Alternativas Ecológicas e Biodegradáveis
Uma nova geração de solventes está emergindo para atender à crescente demanda por produtos mais seguros e sustentáveis. Os bio-solventes, como o lactato de etila e o limoneno, são derivados de fontes renováveis e possuem baixa toxicidade e alta biodegradabilidade.42
Esses solventes ecológicos são projetados para substituir compostos nocivos como thinners, tolueno, xileno e benzeno, oferecendo vantagens de desempenho e segurança.44
A sua composição menos tóxica e o fato de serem, em muitos casos, não inflamáveis, melhoram as condições de saúde e segurança ocupacional, reduzindo os acidentes e a exposição a substâncias perigosas.44
A capacidade de se decomporem naturalmente no ambiente minimiza o acúmulo de resíduos químicos e representa um passo crucial para uma indústria mais responsável.45
📌 7. Conclusão e Recomendações: A Escolha do Veículo Perfeito
O relatório demonstra que a seleção do veículo de limpeza ideal é uma decisão que transcende a mera funcionalidade. A eficácia de uma substância na remoção da sujeira é determinada pela compatibilidade de polaridade, regida pelo princípio fundamental “semelhante dissolve semelhante”.
A água é a escolha natural para sujidades polares, enquanto os solventes apolares são insubstituíveis para óleos, graxas e resinas. Para o desafio comum da limpeza de gordura em ambientes aquosos, a sinergia dos tensoativos, através da redução da tensão superficial e da formação de micelas, se apresenta como a solução química elegante e eficaz.
A decisão final, no entanto, deve ser um processo de múltiplas etapas que inclui a avaliação de riscos e o compromisso com a sustentabilidade. A Ficha de Informações de Segurança de Produto Químico (FISPQ) deve ser consultada para garantir que o manuseio do produto seja feito com o equipamento de proteção e a ventilação adequados.
Adicionalmente, a consideração de alternativas ecológicas e biodegradáveis, bem como a adoção de práticas de reciclagem, são passos cruciais para reduzir o impacto ambiental e os custos de produção.
Para a escolha criteriosa do veículo de limpeza, recomenda-se a seguinte lista de verificação:
– Identifique a Natureza da Sujeira: Determine se a sujeira é predominantemente polar (sal, açúcar) ou apolar (óleo, graxa, verniz).
– Escolha o Solvente Mais Eficaz: Selecione um solvente cuja polaridade seja compatível com a da sujeira. Para misturas, considere o uso de tensoativos.
– Avalie os Fatores de Segurança: Analise a volatilidade, toxicidade e inflamabilidade do produto.
– Consulte a FISPQ/MSDS: Revise o documento para obter informações detalhadas sobre manuseio, armazenamento, EPIs e primeiros socorros.
– Priorize a Sustentabilidade: Se possível, opte por solventes ecológicos ou com potencial de reciclagem para minimizar o impacto ambiental e os custos a longo prazo.
📚 Bibliografia
Brasil Escola. (s.d.). Como as substâncias se dissolvem. Disponível em: https://brasilescola.uol.com.br/quimica/como-as-substancias-se-dissolvem.htm. Acesso em 25 de abril de 2024.8
Brasil Escola. (s.d.). Como o sabão limpa?. Disponível em: https://brasilescola.uol.com.br/quimica/como-sabao-limpa.htm. Acesso em 25 de abril de 2024.14
Brasil Escola. (s.d.). Mistura azeotrópica. Disponível em: https://brasilescola.uol.com.br/quimica/mistura-azeotropica.htm. Acesso em 25 de abril de 2024.46
Brasil Escola. (s.d.). Química dos sabões e detergentes. Disponível em: https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm. Acesso em 25 de abril de 2024.5
Braskem. (s.d.). Tabela de Solventes. Disponível em: https://www.braskem.com.br/portal/Principal/arquivos/listas/12821/thumb.pdf?v=. Acesso em 25 de abril de 2024.47
Clarus Technology. (s.d.). SolvAl® – Linha de solventes ecológicos biodegradáveis. Disponível em: https://brclarus.com/divisao/manufatura/linha/solventes-ecologicos-alternativos-biodegradaveis. Acesso em 25 de abril de 2024.44
Comindex. (s.d.). Bio-solventes derivados do ácido lático. Disponível em: https://www.comindex.es/en/node/1823. Acesso em 25 de abril de 2024.42
Desmold. (s.d.). Thinner de limpeza industrial: dicas de uso. Disponível em: https://www.desmold.com.br/blog/thinner-de-limpeza-industrial/thinner-de-limpeza-industrial-dicas-de-uso/. Acesso em 25 de abril de 2024.25
Desmold. (s.d.). Thinner de limpeza: o que é, aplicações e composição. Disponível em: https://www.desmold.com.br/blog/thinner/thinner-de-limpeza-o-que-e-aplicacoes-e-composicao/. Acesso em 25 de abril de 2024.24
DDS Temas. (s.d.). Como usar solventes inflamáveis. Disponível em: https://ddstemas.com.br/como-usar-solventes-inflamaveis/. Acesso em 25 de abril de 2024.33
DDS Online. (s.d.). Como manusear solventes inflamáveis. Disponível em: https://www.ddsonline.com.br/seguranca/como-manusear-solventes-inflamaveis/. Acesso em 25 de abril de 2024.34
Em-Grade. (s.d.). Ficha de Dados de Segurança (FDS). Disponível em: https://www.em-grade.com/pt-pt/definicoes-de-quimica/msds-sds-fds/. Acesso em 25 de abril de 2024.31
Fq.pt. (s.d.). Pontos de fusão e pontos de ebulição. Disponível em: https://www.fq.pt/tabelas/pontos-de-fusao-e-pontos-de-ebulicao. Acesso em 25 de abril de 2024.48
Gov.br. (s.d.). Solventes e exposição no trabalho. Disponível em: https://www.gov.br/inca/pt-br/assuntos/causas-e-prevencao-do-cancer/exposicao-no-trabalho-e-no-ambiente/solventes. Acesso em 25 de abril de 2024.29
Kebo Chemicals. (s.d.). Limpeza à base de solventes. Disponível em: https://www.kebo-chemicals.com/pt/solucoes/limpeza-quimica/limpeza-a-base-de-solvente/. Acesso em 25 de abril de 2024.23
Khan Academy. (s.d.). Água como solvente. Disponível em: https://pt.khanacademy.org/science/biology/water-acids-and-bases/hydrogen-bonding-in-water/a/water-as-a-solvent. Acesso em 25 de abril de 2024.2
Khan Academy. (s.d.). Solubilidade de compostos orgânicos. Disponível em: https://pt.khanacademy.org/science/organic-chemistry/gen-chem-review/electronegativity-polarity/v/solubility-of-organic-compounds-redo. Acesso em 25 de abril de 2024.7
Mundo Educação. (s.d.). Polaridade das moléculas. Disponível em: https://mundoeducacao.uol.com.br/quimica/polaridade-das-moleculas.htm. Acesso em 25 de abril de 2024.9
Planejativo. (s.d.). Química: propriedades físicas e químicas dos compostos orgânicos. Disponível em: https://app.planejativo.com/estudar/539/resumo/quimica-propriedades-fisicas-e-quimicas-dos-compostos-organicos. Acesso em 25 de abril de 2024.1
Prefeitura de SP. (s.d.). Intoxicação por produtos de limpeza. Disponível em: https://prefeitura.sp.gov.br/web/saude/w/vigilancia_em_saude/doencas_e_agravos/centro_de_intoxicacao/297708. Acesso em 25 de abril de 2024.32
Recom Resíduos. (s.d.). O guia completo para o descarte de solventes. Disponível em: https://www.recomresiduos.com.br/blog/categorias/artigos/o-guia-completo-para-o-descarte-de-solventes-conheca-as-melhores-praticas. Acesso em 25 de abril de 2024.35
Recom Resíduos. (s.d.). Reciclagem de solventes: benefícios e métodos eficazes. Disponível em: https://www.recomresiduos.com.br/blog/categorias/artigos/reciclagem-de-solventes-benef-iacute-cios-e-m-eacute-todos-eficazes. Acesso em 25 de abril de 2024.38
Reddit. (s.d.). Could someone explain why the mantra “like dissolves like” works?. Disponível em: https://www.reddit.com/r/askscience/comments/1f2gup/could_someone_explain_why_the_mantra_like/?tl=pt-br. Acesso em 25 de abril de 2024.3
Reddit. (s.d.). Isopropyl alcohol to remove grease?. Disponível em: https://www.reddit.com/r/AskCulinary/comments/a0yg5o/isopropyl_alcohol_to_remove_grease/?tl=pt-br. Acesso em 25 de abril de 2024.20
Scribd. (s.d.). Tabela Solventes. Disponível em: https://pt.scribd.com/document/546467872/tabela-solventes. Acesso em 25 de abril de 2024.49
Universidade Federal de Juiz de Fora (UFJF). (s.d.). Laboratório de Química dos Elementos – Sabões e Detergentes. Disponível em: https://www2.ufjf.br/quimica/files/2015/10/LABORAT%C3%93RIO-DE-QU%C3%8DMICA-DOS-ELEMENTOS-QUI081-2017-SAB%C3%95ES-E-DETERGENTES-1.pdf. Acesso em 25 de abril de 2024.12
Wikipedia. (s.d.). MSDS. Disponível em: https://pt.wikipedia.org/wiki/MSDS. Acesso em 25 de abril de 2024.30
Referências citadas
Resumo de Propriedades físicas e químicas dos compostos orgânicos, acessado em agosto 30, 2025, https://app.planejativo.com/estudar/539/resumo/quimica-propriedades-fisicas-e-quimicas-dos-compostos-organicos
Propriedades solventes da água (artigo) – Khan Academy, acessado em agosto 30, 2025, https://pt.khanacademy.org/science/biology/water-acids-and-bases/hydrogen-bonding-in-water/a/water-as-a-solvent
Alguém poderia explicar por que o mantra “semelhante dissolve semelhante” funciona? O que exatamente está acontecendo em escala molecular? : r/askscience – Reddit, acessado em agosto 30, 2025, https://www.reddit.com/r/askscience/comments/1f2gup/could_someone_explain_why_the_mantra_like/?tl=pt-br
Respostas do Flexi – A água é um solvente polar ou não polar? | CK-12 Foundation, acessado em agosto 30, 2025, https://www.ck12.org/flexi/pt-br/ciencias-fisicas/concentracao/a-agua-e-um-solvente-polar-ou-nao-polar/
Química dos sabões e detergentes. Atuação dos sabões e …, acessado em agosto 30, 2025, https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm
Você sabe por que a água e o óleo não se misturam? – Mega Curioso, acessado em agosto 30, 2025, https://www.megacurioso.com.br/fisica-e-quimica/85797-voce-sabe-por-que-a-agua-e-o-oleo-nao-se-misturam.htm
Solubilidade de compostos orgânicos (vídeo) | Khan Academy, acessado em agosto 30, 2025, https://pt.khanacademy.org/science/organic-chemistry/gen-chem-review/electronegativity-polarity/v/solubility-of-organic-compounds-redo
Como as substâncias se dissolvem – Brasil Escola – UOL, acessado em agosto 30, 2025, https://brasilescola.uol.com.br/quimica/como-as-substancias-se-dissolvem.htm
Polaridade das moléculas: o que é, resumo – Mundo Educação, acessado em agosto 30, 2025, https://mundoeducacao.uol.com.br/quimica/polaridade-das-moleculas.htm
Por que “Semelhante Dissolve Semelhante”? Entenda de Vez a Solubilidade com Exemplos Incríveis! – YouTube, acessado em agosto 30, 2025, https://m.youtube.com/watch?v=ZTmL-8PzLE4
Água e óleo não se misturam? Descubra se é mito ou verdade. | Blog Europa, acessado em agosto 30, 2025, https://www.europa.com.br/blog/agua-e-oleo-nao-se-misturam
Laboratório de Química dos Elementos – QUI081 – UFJF, acessado em agosto 30, 2025, https://www2.ufjf.br/quimica/files/2015/10/LABORAT%C3%93RIO-DE-QU%C3%8DMICA-DOS-ELEMENTOS-QUI081-2017-SAB%C3%95ES-E-DETERGENTES-1.pdf
SOAP | How do they work in cleaning? – YouTube, acessado em agosto 30, 2025, https://www.youtube.com/watch?v=4oB0v2Q9d7k
Como o sabão limpa? – Brasil Escola – UOL, acessado em agosto 30, 2025, https://brasilescola.uol.com.br/quimica/como-sabao-limpa.htm
Emulsificantes: tipos y aplicaciones, acessado em agosto 30, 2025, https://sip.pochteca.net/index.php/blog/que-son-los-emulsificantes-y-para-que-sirven
Cómo quitar el esmalte semipermanente en casa en 2025 – Perfumerías Primor, acessado em agosto 30, 2025, https://www.primor.eu/blog/como-quitar-unas-semipermanentes/
Fornecedora e distribuidora de solventes – Univar Solutions, acessado em agosto 30, 2025, https://discover.univarsolutions.com/pt-br/chemical-types/solvents/
¿Quitar el esmalte de uñas en inmersión con acetona? : r/Mommit – Reddit, acessado em agosto 30, 2025, https://www.reddit.com/r/Mommit/comments/10pmaqq/removing_dip_nail_polish_with_acetone/?tl=es-es
Como tirar gordura do fogão de um jeito fácil – TudoGostoso, acessado em agosto 30, 2025, https://www.tudogostoso.com.br/noticias/como-tirar-gordura-do-fogao-de-um-jeito-facil-a6315.htm
Álcool isopropílico para remover gordura? : r/AskCulinary – Reddit, acessado em agosto 30, 2025, https://www.reddit.com/r/AskCulinary/comments/a0yg5o/isopropyl_alcohol_to_remove_grease/?tl=pt-br
Vantagens da limpeza com vinagre e bicarbonato | Tenda Atacado, acessado em agosto 30, 2025, https://www.tendaatacado.com.br/dicas/limpeza-com-vinagre-e-bicarbonato/
Vinagre e bicarbonato de sódio como alternativa de limpeza : r/Frugal – Reddit, acessado em agosto 30, 2025, https://www.reddit.com/r/Frugal/comments/9e8utl/vinegar_and_baking_soda_as_a_cleaning_alternative/?tl=pt-br
Limpeza à base de solvente – Keller & Bohacek GmbH & Co. KG, acessado em agosto 30, 2025, https://www.kebo-chemicals.com/pt/solucoes/limpeza-quimica/limpeza-a-base-de-solvente/
Thinner de limpeza: o que é, aplicações e composição – Desmold, acessado em agosto 30, 2025, https://www.desmold.com.br/blog/thinner/thinner-de-limpeza-o-que-e-aplicacoes-e-composicao/
Thinner de limpeza industrial: dicas de uso – Desmold, acessado em agosto 30, 2025, https://www.desmold.com.br/blog/thinner-de-limpeza-industrial/thinner-de-limpeza-industrial-dicas-de-uso/
Riscos dos Solventes – Heitor Borba Soluções, acessado em agosto 30, 2025, https://heitorborbasolucoes.com.br/wp-content/uploads/2013/07/Exposi%C3%A7%C3%A3o-ocupacional-a-solventes.pdf
Saiba como os solventes podem ser uma fonte de contaminação – AmbScience, acessado em agosto 30, 2025, https://ambscience.com/solventes-contaminacao/
Toxicidade dos Solventes em Contexto Laboral – RPSO – Revista Portuguesa de Saúde Ocupacional, acessado em agosto 30, 2025, https://www.rpso.pt/toxicidade-dos-solventes-em-contexto-laboral/
Solventes — Instituto Nacional de Câncer – INCA – Portal Gov.br, acessado em agosto 30, 2025, https://www.gov.br/inca/pt-br/assuntos/causas-e-prevencao-do-cancer/exposicao-no-trabalho-e-no-ambiente/solventes
MSDS – Wikipédia, a enciclopédia livre, acessado em agosto 30, 2025, https://pt.wikipedia.org/wiki/MSDS
MSDS – SDS – FDS ? – EM Grade, acessado em agosto 30, 2025, https://www.em-grade.com/pt-pt/definicoes-de-quimica/msds-sds-fds/
Saneantes domésticos: cuidado na hora da limpeza – Secretaria Municipal da Saúde – Prefeitura de São Paulo, acessado em agosto 30, 2025, https://prefeitura.sp.gov.br/web/saude/w/vigilancia_em_saude/doencas_e_agravos/centro_de_intoxicacao/297708
Como Utilizar Solventes Inflamáveis com Segurança – agosto 2025 – DDS TEMAS, acessado em agosto 30, 2025, https://ddstemas.com.br/como-usar-solventes-inflamaveis/
Como manusear solventes inflamáveis – DDS Online, acessado em agosto 30, 2025, https://www.ddsonline.com.br/seguranca/como-manusear-solventes-inflamaveis/
O Guia Completo para o Descarte de Solventes: Conheça as Melhores Práticas, acessado em agosto 30, 2025, https://www.recomresiduos.com.br/blog/categorias/artigos/o-guia-completo-para-o-descarte-de-solventes-conheca-as-melhores-praticas
Procedimentos para Tratamento e Disposição Final de Resíduos Químicos – ICB-USP, acessado em agosto 30, 2025, https://ww3.icb.usp.br/wp-content/uploads/2019/11/Procedimentos_Tratamento_Disposicao_Final_Residuos_Quimicos.pdf
Impacto ambiental da recuperação de solventes no setor industrial – Os recicladores de solventes para exportação para a Malásia foram enviados, acessado em agosto 30, 2025, https://pt.solventrecyclingsystem.com/news/environmental-impact-of-solvent-recovery-in-th-72494560.html
Reciclagem de Solventes: Benefícios e Métodos Eficazes – Recom Resíduos, acessado em agosto 30, 2025, https://www.recomresiduos.com.br/blog/categorias/artigos/reciclagem-de-solventes-benef-iacute-cios-e-m-eacute-todos-eficazes
COMPARAÇÃO ENTRE OS MÉTODOS DE RECUPERAÇÃO DE SOLVENTE INDUSTRIAL POR DESTILAÇÃO SIMPLES E FRACIONADA, acessado em agosto 30, 2025, https://repositorio.utfpr.edu.br/jspui/bitstream/1/16555/1/PG_COENQ_2017_2_06.pdf
Sistemas de destilação | SCHRADER, acessado em agosto 30, 2025, https://www.schrader.de/pt-br/servicos/sistemas-de-destilacao/
Coleta e Destilação – Reciclagem de Tintas e Solventes em Curitiba – Saturno Química, acessado em agosto 30, 2025, https://saturnoquimica.com.br/servicos/coleta-e-destilacao/
Bio-solventes ecológicos para a indústria – Comindex, acessado em agosto 30, 2025, https://www.comindex.es/en/node/1823
www.conedu.com.br ALTERNATIVAS PARA SOLVENTES MAIS SEGUROS NAS ATIVIDADES DE ENSINO E PESQUISA EM LABORATÓRIO – editora realize, acessado em agosto 30, 2025, https://editorarealize.com.br/editora/anais/conedu/2017/TRABALHO_EV073_MD1_SA19_ID7477_11102017083534.pdf
Solventes Ecológicos Alternativos e Biodegradáveis – CLARUS …, acessado em agosto 30, 2025, https://brclarus.com/divisao/manufatura/linha/solventes-ecologicos-alternativos-biodegradaveis
Solventes ecológicos: importância e benefícios na indústria química – Aromat, acessado em agosto 30, 2025, https://aromat.com.br/blog/solvente-ecologico/
Mistura azeotrópica – Brasil Escola – UOL, acessado em agosto 30, 2025, https://brasilescola.uol.com.br/quimica/mistura-azeotropica.htm
Braskem Solventes, acessado em agosto 30, 2025, https://www.braskem.com.br/portal/Principal/arquivos/listas/12821/thumb.pdf?v=
fq.pt — Pontos de fusão e pontos de ebulição, acessado em agosto 30, 2025, https://www.fq.pt/tabelas/pontos-de-fusao-e-pontos-de-ebulicao
Tabela Solventes | PDF | Química | Ciências Físicas – Scribd, acessado em agosto 30, 2025, https://pt.scribd.com/document/546467872/tabela-solventes
Glossário:
Polaridade Molecular: Propriedade de uma molécula que resulta em uma distribuição assimétrica de cargas, com regiões parcialmente positivas e negativas. É o princípio fundamental que define como as substâncias interagem e se dissolvem.
Solubilidade: A capacidade de uma substância (soluto) se dissolver em outra (solvente). É regida pela regra “semelhante dissolve semelhante”, onde compostos polares se dissolvem em solventes polares, e apolares em apolares.
Solvente Polar: Substância com moléculas polares, como a água, que é capaz de dissolver compostos iônicos e polares. O álcool e a acetona são exemplos de solventes polares orgânicos.
Solvente Apolar: Substância com moléculas apolares, como os óleos, graxas e o thinner, que são eficazes na remoção de sujidades não polares.
Princípio “Semelhante Dissolve Semelhante”: Regra fundamental da química que explica a solubilidade. Ele afirma que as substâncias se dissolvem mais facilmente em solventes com características de polaridade semelhantes às suas.
Tensoativos (ou Surfactantes): Moléculas anfifílicas, como as de sabões e detergentes, que possuem uma parte polar e outra apolar. Elas reduzem a tensão superficial da água e permitem a remoção de gorduras e óleos por meio da formação de micelas.
Micelas: Estruturas esféricas microscópicas formadas por tensoativos em solução aquosa. A parte apolar da molécula se agrupa no interior, aprisionando a sujeira gordurosa, enquanto a parte polar fica em contato com a água, permitindo que a sujeira seja suspensa e removida.
FISPQ (Ficha de Informações de Segurança de Produto Químico): Documento técnico e legal que fornece informações detalhadas sobre os riscos de um produto químico, incluindo dados toxicológicos, procedimentos de manuseio seguro, armazenamento, descarte e os EPIs (Equipamentos de Proteção Individual) necessários.
Reciclagem de Solventes: Processo sustentável de recuperação de solventes usados, geralmente por destilação, para que possam ser reutilizados. Essa prática contribui para a economia circular, reduzindo o volume de resíduos perigosos e o consumo de energia.
Economia Circular: Modelo econômico que visa manter o uso contínuo de materiais e recursos, prolongando sua vida útil e minimizando o desperdício. A reciclagem de solventes é uma prática alinhada a esse modelo.
Solventes Ecológicos (ou Bio-solventes): Alternativas mais seguras e sustentáveis a solventes tradicionais, como o thinner. São derivados de fontes renováveis, possuem baixa toxicidade e são biodegradáveis.
VOCs (Compostos Orgânicos Voláteis): Poluentes atmosféricos nocivos, presentes nos vapores de muitos solventes, que podem ter efeitos negativos na saúde humana e no meio ambiente.